
因此,持续工艺确认(CPV)的核心目标是通过商业规模生产中的持续监控与数据分析,确保工艺始终处于“受控状态”。

雷昶科技提供了一套完整的LC-iCPV全生命周期解决方案,聚焦生产工艺数据智能分析,识别潜在趋势和变异,以闭环式工艺持续确认与改进,切实提升产品合格率、降低生产成本和质量风险。
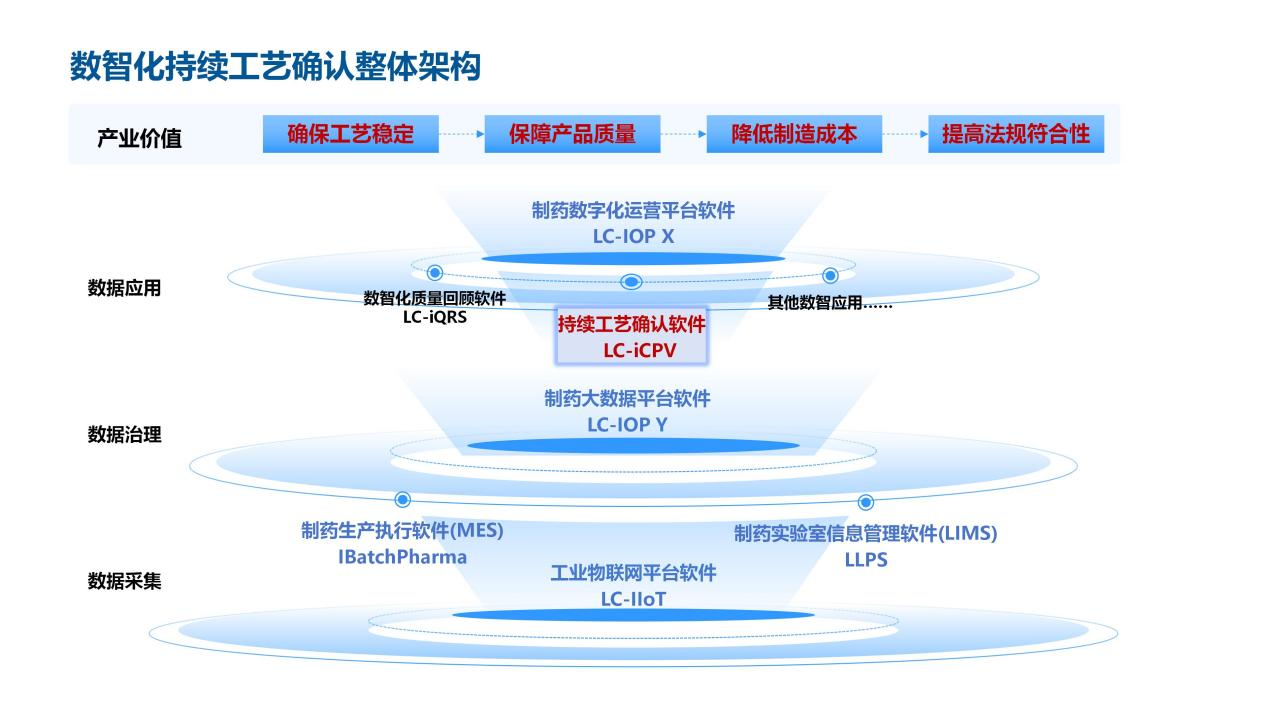
CPV对制药集团管理的意义
1、实现卓越运营
提升生产效率与产能,减少批次失败;
降低生产成本:物料、能源、人力节约;
加速技术转移与工艺放大;
……
2、构建稳健的质量体系
大幅提升法规符合性水平;
质量风险管理变革,转为事前预警与预防,减少事后调查;
为工艺变更和验证提供坚实基线;
……
3、管理协同:
提升整体管控力,便于横向对比、调配资源,实现全面提升;
沉淀与传承工艺知识,积累宝贵的数据资产;
打造核心竞争力,助力通过国际审计;
咨询热线:021-66790312 立即咨询